Je jisté, že významnou roli sehrál postoj kontinentální Číny, která už od března 2019 o struktuře existujícího nebezpečného viru věděla / prosáklo to díky odvaze jednoho čínského vědce už v létě na virologicko – imunologické symposium. Ale, jak to na kongresech bývá, večernímu satelitnímu zasedání, jichž se zúčastnilo několik pospávajících lidí, nikdo nevěnoval pozornost. Přitom každý zkušený strukturální virolog musí díky struktuře regulačního genu, která je unikátní, a díky současné přítomnosti dvou genů / vazba na ACE 2 a transmembránovou proteinasu /, které se v přírodě vedle sebe nevyskytují, tomuto viru věnovat ihned zvýšenou pozornost. Proč se tyto geny nevyskutuji současně? Protože jsou charakteristická pro dva živočichy, netopýra a luskouna ostrovního, kteří ani ve stejném ekosystému spolu nežijí a míjejí se v čase i v prostoru.
Údajně první infikovaný / hledaný ! / pacient byl objeven v Číně 17. listopadu 2019, pak tam nastalo peklo, jehož existenci kontinentální Číňané prakticky až do konce ledna 2019 tajili stejně jako strukturu viru. Samozřejmě tehdy uváděná mortalita 4 – 6% sloužila i ke zdůvodnění represivních opatření a sama asi byla důsledkem zvýšené úmrtnosti např. v důsledku velmi špatných ekonomických podmínek. Bagatelizovat COVID-19 by bylo totéž jako bagatelizovat existenci nebezpečného SARS a MERS, se kterými však je není možné srovnávat, protože se z epidemiologického hlediska chovají zcela odlišně – kdo byl infikovaný, vážně onemocněl, a tudíž bylo možné obě onemocnění snadno limitovat, příprava vakcíny na SARS byla dokonce zastavena.
Zrádnost tohoto nového koronaviru SARS-CoV-2 spočívá v tom, že až 80 – 90 infikovaných lidí může být víceméně klinicky asympomatických / případně drobné respirační příznaky jako u 4 druhů koronavirů, které zde tisíce let v naší populaci cirkulují a působí onemocnění připomínající “ nachlazení „, přičemž prokázaní infikovaní lidé i lidé, kteří ještě ani test nemají pozitivní, mohou být masivními nosiči. Z epidemiologického hlediska se tedy tento virus chová jako chřipka a prakticky nejsme schopni ho lokalizovat. Díky své virové struktuře / zcela bez obdoby v přírodě je regulační gen, dále gen pro receptor vážící se s molekulou ACE 2 a s transmembránovou serinovou proteázou / proniká do nejrůznějších cílových buněk lidského těla, díky šíření kapénkovou infekcí především do dýchacích cest, zejména do distálních dýchacích cest a alveolů / pneumocyty II. typu /.
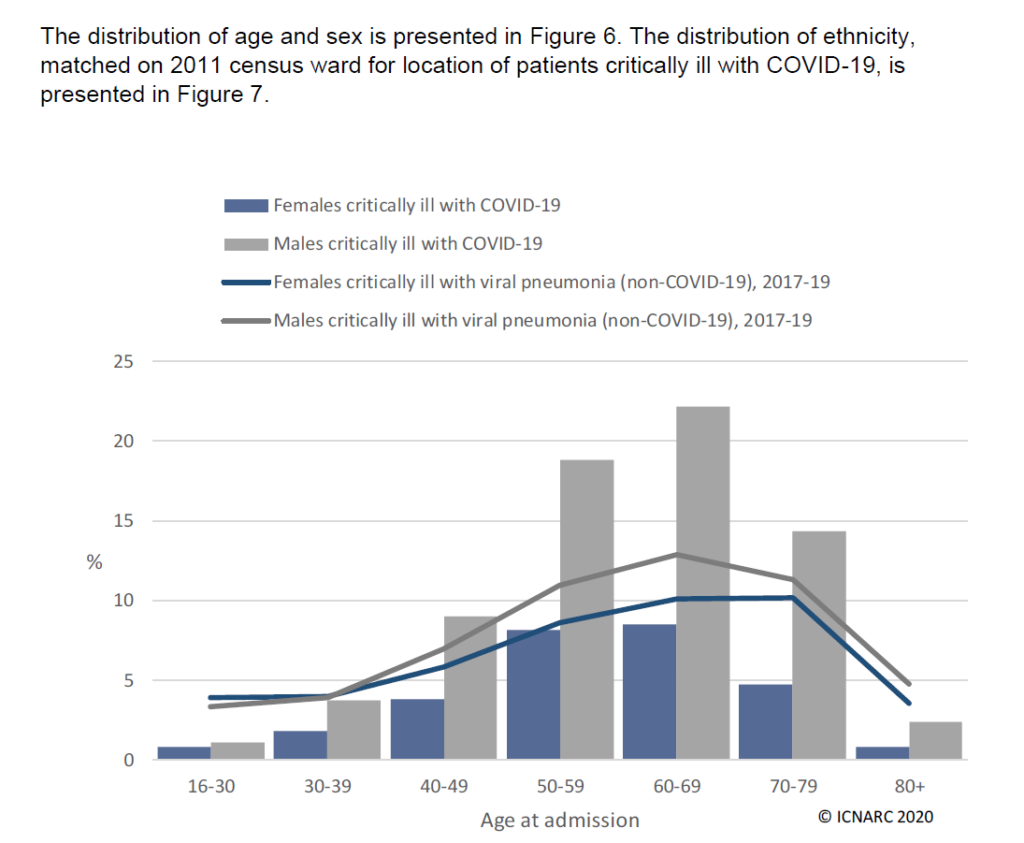
Molekula ACE má svouji “ vnitřní logiku “ – vyvolává vzestup TK a především vazokonstrikci s možným následným hypoxickým poškozením tkání, včetně generalizované endotelitidy a následné endoteliální dysfunkce, ale zároveň prostřednictvím regulace funkce gama Interferonu, jehož změny pozoroji při zvýšení či snížení sérového angiotensin konvertujícího enzymu v séru, již asi 5 – 6 let, “ zvýšení SACE – zvýšení gama IFN a obráceně. Transmembránová serinová proteinasa je regulována testosteronem, proto se asi mapa variant Y chromosomu v Evropě kryje s místem vyššího a nižšího výskytu těžkých forem COVIDU-19 / “ hranice na Rýnu “ /. Řada studií svědčí pro to, že muži léčení pro onemocnění prostaty inhibitory testosteronu, mají podstatně redukovanou možnost onemocnění COVIDEM-19.
Při aktivaci ACE 2 dochází nejdříve i při respirační formě COVIDU-19 k lokální vazokonstrikce a hypoxii, asi v 10% případů se však reakce generalizuje, postihuje prakticky všechny endothelie / endotelitis / trpící potom hypoxií, rozvíjí se endoteliální dysfunkce, cirkulující imunokomplexy tvořené protilátkou proti novému koronaviru a koronavirem nejsou v důsledku redukované funkce T lymfocytů fagocytovány, selhává fagocytární clearence, a imunokomplexy jsou deponovány do tkání, především do cévní stěny, kde indukuje vaskulitidu, pozměněná vnitřní cévní stěna pak indukuje i tvorbu autoprotilátek, především různé formy antifosfolipidových a antikardiolipinových autoprotilátek, které přispívají k vzniku tepenných i žilních trombů a embolů, po konsumpci srážecích faktorů pak se rozvíjí i disseminovaná intravaskulární koagulace / DIC / a za přispění SIRS a CARS dochází k extrémní tvorbě cytokinů, a to nekoordinovaně a jednotlivé cytokiny mají často i protichůdné účinky. Samozřejmě podobná imunopatologická reakce zabíjí infikované lidi i při jiných infekcích / “ odpověď organizmu “ /, ale zde je díky zapojeným imunologickým funkcím a zvláštní struktuře viru zcela odlišná.
Zradou COVIDu-19 je jednak jeho nevyzpytatelné epidemiologické chování, u 80 – 90% lidí nejsme prakticky schopni infekci zachytit / asymptomatičí nebo tzv. “ respirační forma “ /, u asi 10% lidí těžká, život ohrožující “ vaskulární forma „, která může skončit, zejména u predisponovaných / určitá onemocnění, genetický polymorfizmus,../ fatálně. Proč právě u těchto lidí, to nevíme. Studie z poslední doby ukazují, že u lidí, kteří prodělali infekci SARS-CoV-2, se u helper CD4+ T lymfocytů a u aktivovaných CD8+ cytotoxických T lymfocytů vytváří specifický receptor pro SARS-CoV-2, ale překvapením je, že i u lidí, kteří COVID-19 neprodělali, nacházíme si u 40 – 60% lidí tyto receptory na stejných typech CD lymfocytárních subpopulací. Snad je o zkříženou reakci s běžnými, v našem prostředí přítomnými, koronaviry, které nejsou nadány schopností indukovat onu “ vaskulární fázi “ /
Další otázkou jsou i mezi lymfocytárními receptory existující antiidiotypové sítě, podobně jako u protilátek, kdy každá lichá generace je namířena proti antigenu, tedy zde viru, každá sudá generace je “ vnitřním obrazem “ antigenu, tedy viru, se kterým se organizmus setkal tyto “ vnitřní obrazy mají pravděpodobně i určitý imunogenní potenciál ! Ale to už je trochu scifi.